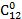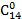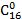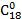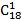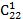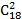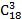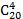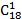4.2 Теоретичні відомості
Класифікація, будова та значення ліпідів
Харчові жири – це продукти харчування, які одержують з жирових тканин рослинних та тваринних організмів. Жири відносять до найважливіших складових харчування. Жирові та жировмісні продукти є постійною складовою раціону людини.
В організм людини з продуктами харчування жири надходять, так званими, "видимими" (олія, вершкове масло, сало тощо) та "прихованими" (риба, м’ясо, молоко, яйця). Доросла людина повинна споживати приблизно 32 кг жиру на рік, половина якого має припадати на "видимий".
Роль жирів у харчуванні людини:
1) вони є основним джерелом енергії – 1 г жирів дає організму 37,7 кДж (середня норма енергії складає 11,7 кДж/добу). Енергетичні витрати людини забезпечуються за рахунок жирів приблизно на 33%;
2) жири, що входять до складу кліткових мембран – так звані, структурні жири, беруть участь у пластичних процесах організму – будові та оновленні всіх його тканин;
3) резервні жири, що відкладаються у спеціальних жирових клітинах є "запасним джерелом енергії" й використовуються організмом за нестачі їжі.
4) жири є постачальниками біологічно-активних речовин: незамінних поліненасичених кислот, різних форм вітаміну А (рибофлавіну), вітаміну Д (кальциферолу), вітаміну Е (токоферолу), фосфоліпідів, стеринів;
5) підшкірна жирова тканина оберігає організм людини від надмірної тепловіддачі (терморегуляторна функція); жири внутрішніх органів є своєрідними амортизаторами для них;
6) складові жирів сприяють виділенню жовчі, накопиченню білків в організмі;
Систематична нестача жирів у харчуванні скорочує життя, порушує діяльність нервової системи, знижує стійкість до різних захворювань. Водночас, надлишок жирів у харчуванні призводить до ожиріння, атеросклерозу, розвитку жовчнокам’яної хвороби, виникненню злоякісних новоутворень у молочних, статевих залозах, прямій кишці тощо.
Існують науково обґрунтовані і перевірені медичною практикою норми споживання жирів у грамах для окремих груп населення залежно від віку, статі характеру праці тощо. Середня потреба дорослої людини у жирах складає 90 г на добу, причому у такому співвідношенні: 20...35% олії, 25% вершкового масла, 40...50% маргарину, кулінарних жирів.
Жирами називають групу харчових продуктів – рослинні олії, тваринні топлені жири, маргарин, вершкове масло, жири для кулінарії, кондитерської та хлібопекарної промисловості. Більш загальна й правильна назва жирів – ліпіди (від грец. – lipos – жир).
Ліпіди – це група органічних сполук, що хімічним складом є похідними жирних кислот, спиртів, альдегідів, побудованих за допомогою етерного, естерного, фосфороетерного та глікозидного зв'язків, спільними властивостями яких є нерозчинність у воді та здатність розчинятися в органічних розчинниках.
Класифікація ліпідів наведена на схемі рисунку 4.1.
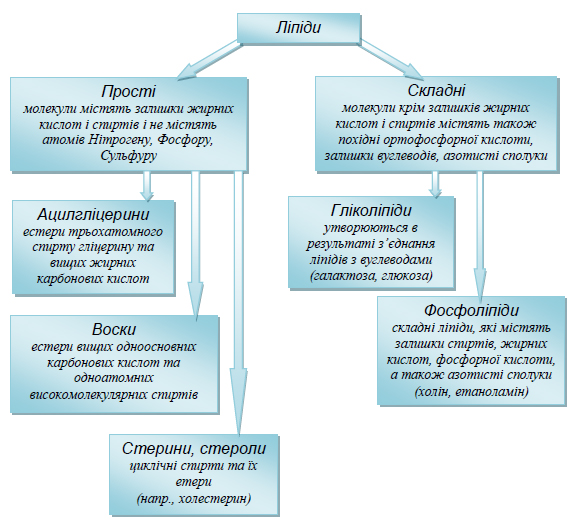
Рисунок 4.1 – Класифікація ліпідів
Ліпіди широко розповсюджені у природі, разом з білками і вуглеводами вони складають основну масу органічних речовин усіх живих організмів і є обов'язковим компонентом кожної клітини. У рослинах ліпіди накопичуються, головним чином, в насінні і плодах. Вегетативні частини рослин накопичують до 5% ліпідів, насіння – до 50%. Вміст ліпідів в тушці риб (осетрів) може досягати 20...25%, в оселедці – 10%, у наземних тварин воно сильно коливається: 33% – свинина, 9,8% – яловичина; у молоці оленя – 17...18%, кози – 5%, корови – 3,5...4,0% ліпідів, у м'ясі міститься від 1 до 50% ліпідів.
Серед гліцеридів розрізняють моно-, ді-, тригліцериди. Моно- і дігліцериди у природі трапляються досить рідко. Основним компонентом харчових жирів є тригліцериди. Вони не мають смаку і запаху, безбарвні. До складу молекули тригліцеридів харчових жирів входять: гліцерин (близько 10%) і жирні кислоти з різною довжиною вуглецевого ланцюга та різним ступенем насиченості атомів вуглецю (насичені й ненасичені жирні кислоти). Жирні кислоти, які входять до складу ліпідів, містять, переважно, парну кількість атомів карбону, найчастіше – 16 або 18.
Кожний вид жиру має тригліцериди, до складу яких входить певний набір жирних кислот (таблиця 4.1). Тому різні види олій, тваринних топлених жирів мають постійні, притаманні тільки їм фізико-хімічні (температура топлення, твердість, здатність до окиснення), органолептичні (смак, запах, консистенція) показники, біологічну цінність та засвоюваність. Тобто жирокислотний склад тригліцеридів вирішальним чином впливає властивості жирів.
Таблиця 4.1 – Основні карбонові кислоти, що входять до складу природних олій і жирів
|
Кислота |
Формула |
Символ* |
|
Насичені кислоти |
||
|
Лауринова |
CH3-(CH2)10 - COOH |
|
|
Міристинова |
CH3-(CH2)12 - COOH |
|
|
Пальмітинова |
CH3-(CH2)14 - COOH |
|
|
Стеаринова |
CH3-(CH2)16 - COOH |
|
|
Ненасичені кислоти |
||
|
Олеїнова |
CH3-(CH2)7-CH=CH-(CH2)7-COOH |
|
|
Ерукова |
CH3-(CH2)7-CH=CH-(CH2)11-COOH |
|
|
Лінолева |
CH3-(CH2)4-CH=CH-CH2-CH=CH-(CH2)7-COOH |
|
|
Ліноленова |
CH3-(CH2-СН=СН)3-(СН2)7-СООН |
|
|
Арахідонова |
СН3-(СН2)3-(СН-СН=СН)4-(СН2)3-СООН |
|
|
Оксикислоти |
||
|
Рициноленова |
СН3-(СН2)5-СНОН-СН2-СН=СН-(СН2)7-СООН |
|
*Примітка. У символ входять число атомів вуглецю і кількість подвійних зв'язків між вуглецевими атомами в молекулі кислоти, номер першого ненасиченого атома вуглецю і конфігурація.
Так, до складу ацилгліцеринів тканинних жирів (яловичий, баранячий, свинячий, курячий, молочний) входять в основному жирні кислоти, що містять 16...18 вуглецевих атомів (пальмітинова, стеаринова, олеїнова, лінолева, ліноленова). У меншій кількості у складі ацилгліцеринів представлені жирні кислоти, що містять від 2 до 14 або від 20 до 22 вуглецевих атомів. Ці одноосновні кислоти можуть бути насиченими і ненасиченими. У тваринних жирах міститься більше насичених кислот, в рослинних (ненасичених (олеїнової С 18:1, лінолевої С 18:2, ліноленової С 18:3, арахидонової С 20:4). Важливе біологічне значення мають ті ненасичені жирні кислоти з 18 вуглецевими атомами.
Жирні кислоти насичені (масляна, капронова, пальмітинова, стеаринова тощо) використовуються організмом в цілому як енергетичний матеріал. Вони є твердими за консистенцією за температури 18°С, мають високу температуру плавлення (44...75°С). У більшості насичені жирні кислоти містяться в тваринних жирах (яловичому, баранячому).
Жирні кислоти ненасичені (олеїнова, ерукова, лінолева тощо) містяться в основному у рослинних оліях, є рідкими за консистенцією, мають низьку температуру плавлення й, відповідно, легше засвоюються організмом людини, ніж насичені жирні кислоти.
Радикали ненасичених жирних кислот є хімічно активними. За місцем кратних зв’язків вони вступають в реакції приєднання, окиснення, полімеризації. Тому їх можна якісно виявити за допомогою бромної води (реакція приєднання), знебарвлення розчину перманганату калію (реакція окиснення).
Ненасичені кислоти мають різний ступінь ненасиченості (кількості подвійних зв'язків між атомами вуглецю): олеїнова – 1, лінолева – 2, ліноленова – 3, арахідонова – 4 (рисунок 4.2). Кожна з перелічених кислот має різну здатність приєднувати кисень ( окиснюватись).
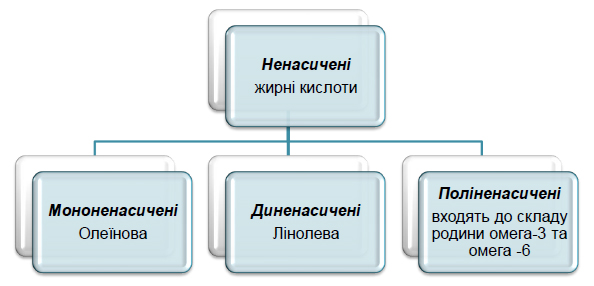
Рисунок 4.2 – Класифікація ненасичених жирних кислот
Чим більше в жирах ненасичених кислот, особливо з 3, 4, 5 подвійними зв'язками, тим жир швидше окислюється, тобто гіркне, осалюється. Тому під час зберігання жирів потрібно стежити, щоб вони не контактували з повітрям, залізом, міддю, цинком. Також необхідно дотримуватись встановлених нормативно-технічною документацією температурних режимів та термінів зберігання жирів.
Особливе значення мають поліненасичені жирні кислоти – ліноленова, арахідонова, клупанодонова та інші, які не можуть синтезуватися в організмі людини і тому є незамінними, як є незамінними деякі амінокислоти та вітаміни.
Олії порівняно з тваринними плавленими жирами вважаються біологічно ціннішими, оскільки в них більшій вміст ненасичених жирних кислот, у т.ч. незамінних поліненасичених.
Позитивний вплив поліненасичених жирних кислот на функціонування організму людини проявляється в наступному:
– регулюють обмін холестерину: за недостатньому їх вмісті відбувається етерифікація холестерину з насиченими кислотами, що призводить до розвитку атеросклерозу. Ненасичені кислоти перетворюють холестерин у фолієві кислоти і виводять його з організму;
– регулюють розвиток організму: за їх недостатнього вмісту знижуються темпи росту організму і його стійкість до ультрафіолетового та радіактивного опромінення;
– підвищують еластичність кровоносних судин.
Але незважаючи на безперечну користь жирів для організму, існує небезпека його перевантаження жиромівмісними продуктами харчування, оскільки надлишок у харчуванні поліненасичених кислот призводить до виникнення захворювань нирок і печінки.
Надлишок у харчуванні насичених кислот призводить до порушення обміну жирів, збільшення рівня холестерину в крові, жовчнокам'яної хвороби, ожиріння.
Оптимальною в біологічному плані формулою збалансованості насичених і ненасичених жирних кислот (молекула ідеального жиру), є співвідношення 30%:70%. До жирів, які за жирнокислотним складом є наближеними до ідеальної формули, належать оливкова, арахісова олія, свинячий топлений жир.
Речовини, супутні гліцеридам
Ліпоїдні речовини у складі жирів. Кількість і вміст речовин, супутніх гліцеридам (ліпоїдних речовин) є непостійними і залежать від якості жирової сировини, технології отримання та ступеню рафінації жирів.
У рослинних оліях на частку ліпоїдних речовин припадає 3...4% маси, в тваринних – у декілька разів менше. Виняток – жири морських тварин та риб, в яких вміст ліпоїдних речовин сягає десятків відсотків. До речовин, супутніх гліцеридам, належать фосфоліпіди, стерини, вільні жирні кислоти, барвникові речовини, вітаміни, воски.
Вільні жирні кислоти в ідеалі не повинні міститись у жирах. Їх наявність свідчить про те, що виготовлення тваринних жирів та їх зберігання відбувалися з порушенням технологічних режимів. Показник, який кількісно характеризує наявність в жирах вільних жирних кислот – кислотне число. Воно нормується стандартами на всі види жирів і від нього залежать сорти тваринних топлених жирів.
Фосфоліпіди (фосфатиди) відіграють важливу роль в організмі людини. Входячи до складу клітинних мембран, вони справляють суттєвий вплив на проникність мембран і обмін речовин між клітинами. Основними фосфоліпідами є лецитин (до складу якого входить вітамінна сполука холін), а також кефалін. Лецитин необхідний для формування клітин і тканин організму, запобігає накопиченню холестерину, сприяє його виведенню, запобігає ожирінню печінки. Лецитин і кефалін є природними емульгаторами та антиокисниками.
Стерини – високомолекулярні спирти, які містяться в тканинах рослин і тварин. За походженням розрізняють:
– зоостерини – стерини тваринного походження (холестерин);
– фітостерини – стерини рослинного походження (ситостерин, стигмастерин);
– мікостерини – стерини грибного походження.
Стерини мають кристалічну будову, причому зоостерини й фітостерини різняться формою кристалів, що дозволяє ідентифікувати природу жиру (встановити його походження).
З тваринних стеринів важливе значення має холестерин. Він є нормальним структурним компонентом усіх клітин і тканин, бере участь в обміні жовчних кислот, синтезі низки гормонів, вітаміну Д (частина якого утворюється під впливом ультрафіолетових променів з того ж холестерину).
Нормальний вміст холестерину в крові становить 1,9...2,1 г/л. Підвищення його рівня до 2,6 г/л є дуже небезпечним – у людини виникає і розвивається атеросклероз, ускладненими наслідками якого є інфаркти, інсульти.
Нестача холестерину в крові (менше 1,5 г/л) викликає ураження наднирників, розростання щитовидної залози. Явна нестача холестерину виявляється у випадку цирозу, інфекційному гепатиті та інших захворюваннях печінки. Близько 80% холестерину утворюється в організмі у печінці та інших органах з насичених жирних кислот. Решта 20% надходить з їжею. Але відповідними дослідженнями встановлено чіткий зв’язок – чим більше холестерину надходить з їжею, тим меншу його кількість синтезує печінка й навпаки.
Склад харчових жирів, що входять до раціону людини може помітно впливати на рівень холестерину в організмі. Якщо в раціоні багато рослинних жирів (олій), то вміст холестерину знижується, якщо споживаються значною мірою тваринні жири, то концентрація холестерину в крові підвищується.
Чистий холестерин – перлинчасті пластинки, жирні на дотик. Він нерозчинний у воді, малорозчинний в органічних розчинниках. Температура плавлення холестерину становить 149°С.
Воски – це складні ефіри високомолекулярних карбонових кислот та одноосновних високомолекулярних спиртів (цетиловий, міристиловий, карнаубіловий і т.д.). За природою всі воски є хімічно інертними. Розрізняють рослинні та тваринні, тверді та м’які воски. Рослинний віск є складною сумішшю органічних сполу з великою масою, він вкриває листя та стебла рослин, зменшуючи випаровування води. Прикладом рослинного воску є карнаубський віск із восконосної пальми карнауби.
Воски тваринного походження:
– бджолиний;
– овечий: виділяється на шкіру та вовну овець і складає 5...10% від маси вовни, його видаляють розчинниками й отримують технічний ланолін, а очищений використовують як сировину для медичних і косметичних мазей, кремів тощо;
– жир кашалотів (спермацетовий жир) на 75% складається з воскоподібної речовини, з нього вилучають віск спермацет, який також є основою для виготовлення окремих видів медичних і косметичних мазей, кремів, а також мила.
Крім восків тваринного і рослинного походження виділяють віск викопного походження (озокерит), який не має жодного відношення до харчової промисловості.
Барвникові речовини містяться здебільшого у рослинних жирах, тваринні жири їх майже не містять. Ці речовини легко руйнуються, окинюючись під дією світла. Найбільш відомі барвникові речовини – це каротиноїди, хлорофіл, госсіпол.
Вітаміни жирів представлені групою жиророзчинних вітамінів А, Д, Е, К.
Фізико-хімічні показники якості жирів
До фізико-хімічних показників якості жирів відносяться наступні: масова частка вологи та летких речовин, кислотне число, пероксидне число, йодне число, кількість антиоксидантів, температура застигання.
Процеси, що відбуваються в ліпідах під час їх зберігання та переробки, характеризуються так званими константами, або хімічними та фізичними числами жиру (мається на увазі витрата певних реагентів на реакції з жиром). Визначення цих констант дає змогу контролювати не тільки якість жирів та олій, але й в певній мірі їх натуральність, регулювати технологічні режими отримання продуктів. Найбільше значення мають такі числа: кислотне, омилення, йодне.
Кислотне числом – показник, що характеризує кількість вільних жирних кислот, які містяться в жирі. Кислотне число – це кількість гідроксиду калію (в мг), витраченого на нейтралізацію вільних жирних кислот, що містяться в 1 г жиру або олії.
Йодне число – показник, що характеризує ненасиченість жирних кислот, що входять до складу жиру. Йодне число – це маса йоду(у г), що приєднується до 100 г жиру. Існує декілька методів його визначення, що відрізняються, в основному, галогеновмісним реагентом.
Число омилення – показник, що характеризує загальну кількість вільних та зв’язаних жирних кислот (у складі естерів), що входять до складу досліджуваного жиру. Число омилення – це кількість міліграм 0, 1н розчину гідроксиду калію, необхідного для омилення гліцеридів і нейтралізацію кислот, що містяться в 1г жиру або олії. Омилення – це гідроліз жирів лугами, внаслідок чого утворюються гліцерин та солі жирних кислот – мила. Число омилення дорівнює сумі кислотного і естерного чисел.
Естерне число – показник, що характеризує вміст естерів у жирі. Естерне число – це кількість міліграмів гідроксиду калію, яка необхідна для омилення всіх естерів, що містяться в 1 г жиру. Естерне число дорівнює різниці між числом омилення і кислотним числом.
Пероксидне число – це кількість грамів йоду, яка виділилася з йодиду калію пероксидними сполуками, що містяться в 100 г жиру. Ця константа вказує на вміст пероксидних сполук у жирі, дозволяє виявити окислювальні процеси та наявність продуктів псування значно раніше, ніж це може бути встановлено органолептично.
Величини розглянутих констант для окремих жирів і олій, що не піддалися руйнуванню, коливаються в незначних межах і характеризують вид жиру і його якість (таблиця 4.2).
Таблиця 4.2 – Вміст жирних кислот(у %) і характеристики олій і жирів
|
Жири та олії |
Вміст і склад жирних кислот |
Характеристика |
|||||
|
Насич. |
Ненасич. |
Основних |
Темпер. застигання |
Число омилення |
Йодне число |
||
|
Олії |
|||||||
|
Соєва |
14...20 |
75...86 |
С |
-18 |
191...193 |
120...140 |
|
|
Бавовняне |
22...30 |
75...76 |
С |
2...4 |
191...198 |
101...116 |
|
|
Соняшникова |
10...12 |
до 90 |
С |
16...18 |
186...194 |
119...136 |
|
|
Рапсове |
2...6 |
94...98 |
С |
0...10 |
167...181 |
94...103 |
|
|
Оливкова |
9...18 |
82...91 |
С |
0...6 |
185...200 |
72...89 |
|
|
Кокосова |
до 90 |
10 |
С С |
16...25 |
251...264 |
7...12 |
|
|
Пальмова |
44...57 |
43...56 |
С С |
31...41 |
196...210 |
52...58 |
|
|
Пальмоядерна |
79...83 |
17...21 |
С |
19...24 |
240...257 |
15...20 |
|
|
Льняне |
6...9 |
91...94 |
С |
18...27 |
191...195 |
175...190 |
|
|
Тваринні жири |
|||||||
|
Яловичий |
45...60 |
43...52 |
С |
30...38 |
190...200 |
32...47 |
|
|
Баранячий |
52...62 |
38...48 |
С С |
32...45 |
192...198 |
31...46 |
|
|
Свинячий |
33...49 |
48...64 |
С |
22...32 |
193...200 |
46...66 |
|
БІОХІМІЧНІ І ФІЗИКО-ХІМІЧНІ ЗМІНИ ЖИРІВ
В процесі переробки і зберігання жировмісних продуктів або виділених з них жирів відбуваються різноманітні перетворення їх під впливом біологічних, фізичних і хімічних чинників.
В результаті цих перетворень змінюється хімічний склад, погіршуються органолептичні показники і харчова цінність жирів, що може привести до їх псування.
Незалежно від технологічних режимів переробки і зберігання, а також виду жиру в них проходять однотипні зміни, що зводяться до гідролізу і окислення. Ці процеси відбуваються за схемою, представленою на рисунку 4.3.
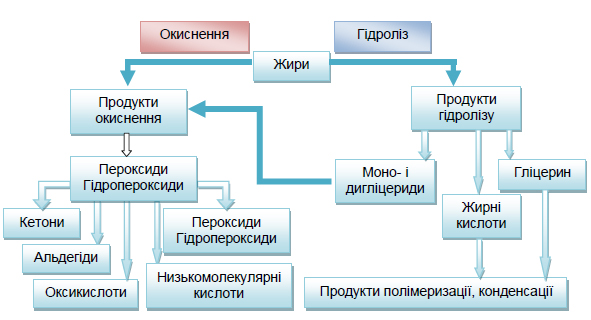
Рисунок 4.3 – Схема перетворення жирів
Переважання в жирі гідролітичного або окислювального процесу залежить від температури, наявності кисню, світла, води, тривалості нагрівання, присутності речовин, що прискорюють або уповільнюють ці процеси. Тому основні способи теплової обробки жировмісних продуктів і жирів (варіння, смаження) розрізняються за ступенем і характером дії на жир. Під час варіння переважають гідролітичні процеси, а в процесі смаження – окиснювальні. У будь-якому випадку якість жиру оцінюють за кислотним, пероксидним, ацетиловим числами, вмістом альдегідів, кетонів та інших сполук.
Гідролітичне розщеплення жирів
Гідролітичне розщеплення жирів проходить за обов'язкової участі води і може бути як ферментативним, так і неферментативним. У тканинних жирах, жирі-сирці (внутрішній жир), жирі м'яса, плодів і овочів, жирі сирокопчених продуктів і т.п. під впливом тканинних ліпаз спостерігається гідроліз ацилгліцеринів, що супроводжується накопиченням жирних кислот і, як наслідок, підвищенням кислотного числа. Швидкість і глибина гідролізу жиру залежать від температури: процес ферментативного каталізу значно прискорюється за температури вище 20ºС; зниження температури уповільнює процес гідролізу, але навіть за -40ºС ферментативна активність ліпаз проявляється, але в слабкій мірі.
За несприятливих умов (волога, підвищена температура) може статися гідролітичне псування жирів, спричинене не лише дією ферментів, але і інших чинників: кислот, лугів, оксидів металів й інших неорганічних каталізаторів, а також ферментів мікроорганізмів.
Утворення в жирі за гідролітичного розпаду невеликої кількості високомолекулярних жирних кислот не викликає змін смаку і запаху продукту. Але якщо у складі тригліцеридів (молочний жир) є низькомолекулярні кислоти, то під час гідролізу можуть з'явитися капронова і масляна кислоти, що характеризуються неприємним запахом і специфічним смаком, які різко погіршують органолептичні властивості продукту.
У топлених жирах автолітичного (ферментативного) розщеплення жирів не спостерігається, оскільки в процесі витоплення за температури близько 60ºС ліпаза, що міститься в жировій тканині, інактивується. Гідролітичне псування топленого жиру відбувається за наявності вологи, в результаті обсіменіння мікрофлорою, неповній денатурації білків при витопленні жиру з жирової тканини або під впливом каталізаторів.
Окислювальні процеси в жирах
В процесі переробки і зберігання жирів можливе погіршення їх якості в результаті окиснювальних процесів, глибина і швидкість яких залежать від природних властивостей жиру, температури, наявності кисню і світла. Ці чинники можуть викликати окислювальне псування жирів.
Розрізняють автоокиснення і термічне окислення жирів. Автоокиснення жирів проходить за низьких температур у присутності газоподібного кисню. Термічне окиснення відбувається за температури 140ºС...200ºС. Між термічним і автоокисненням є багато спільного, проте склад продуктів, що утворюються, дещо відрізняється.
Продукти, що утворюються за автоокиснення і термоокиснення поділяються на три групи:
1) продукти окиснювальної деструкції жирних кислот, в результаті якої утворюються речовини з укороченим ланцюгом;
2) продукти ізомеризації, а також окиснені ацилгліцерини, які містять ту ж кількість вуглецевих атомів, що і початкові ацилгліцерини, але відрізняються від останніх наявністю у вуглеводневих частинах молекул жирних кислот нових функціональних груп, що містять Оксиген.
3) продукти окиснення, що містять полімеризовані або конденсовані жирні кислоти, в яких можуть знаходитися і нові функціональні групи, що мають у своєму складі Оксиген.
Крім того, продукти окиснення поділяють на термостійкі і нетермостійкі.
Первинними продуктами окиснення є пероксиди, що активують окиснення інших молекул. Завдяки цьому реакція окиснення носить ланцюговий характер. Окисненню піддаються в першу чергу ненасичені жирні кислоти, але можуть окислюватися також і насичені кислоти з утворенням гідропероксидів. За глибокого окиснення жирів можливе утворення циклічних пероксидів та епоксидних сполук.
Вміст пероксидних сполук в жирі оцінюють за величиною пероксидного числа. Це досить чутливий показник, і за його значенням роблять висновок про початок і глибину окиснення жиру. У свіжому жирі пероксидів немає. На початкових стадіях окиснення впродовж деякого часу хімічні і органолептичні показники жиру майже не змінюються. Цей період, що має різну тривалість, називається індукційним. Після індукційного періоду жир починає псуватися. Виявити це можна за збільшенням пероксидного числа і зміною органолептичних властивостей жиру.
Наявність індукційного періоду пояснюється тим, що на початку процесу молекул з підвищеною кінетичною енергією (збуджених або вільних радикалів) дуже мало. Зумовлено це також змістом в жирі природних антиокисників: каротиноїдів, токоферолів, лецитинів, які активніше взаємодіють з вільними радикалами і з киснем повітря і тим самим перешкоджають окисленню жирів. Тривалість індукційного періоду залежить від концентрації антиокисників, природи жиру і умов переробки і зберігання. Тваринні жири, у складі яких менше ненасичених жирних кислот, є стійкішими, ніж рослинні.
Процес автоокиснення жирів значно прискорюється за наявності вологи, світла і каталізаторів. Такими каталізаторами можуть бути легкоокиснювальні метали (оксиди або солі Феруму, Купруму, Плюмбуму, Стануму), а також органічні сполуки, що містять Ферум, білки, гемоглобін, цитохроми й інші.
Каталітична дія металів пов’язана з їх здатністю легко приєднувати або віддавати електрони, що призводить до утворення вільних радикалів з гідропероксидів жирних кислот. Активними каталізаторами є ферменти, головним чином ферменти мікроорганізмів. Тому забруднення жирів, особливо бактеріальне обсіменіння, прискорює процес окислення жирів.
Пероксиди і гідропероксиди є нестійкими сполуками тому відбувається їх розпад з утворенням вільних радикалів, наприклад, R-О-О-Н → RО• + •ОН й інших. При цьому проходять подальші різноманітні реакції, в результаті яких накопичуються вторинні продукти: оксисполуки, альдегіди, кетони, низькомолекулярні кислоти й інші.
Під час окиснення жирів виявлений ряд альдегідів, що є продуктами розпаду ланцюга жирних кислот: ноніловий, азолаїновий, гептиловий, малоновий. Подальше перетворення низькомолекулярних альдегідів призводить до появи низькомолекулярних спиртів, жирних кислот і до нового розгалуження окислювального ланцюга.
Кетони, як і альдегіди, утворюються окислювальним шляхом в результаті подальших перетворень пероксидів, наприклад, в результаті їх дегідратації.
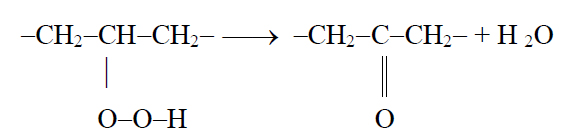
Припускають, що за присутності ферментів мікроорганізмів кетони можуть утворюватися за типом β-окиснення, тобто за участю води.
Псування жирів: згіркнення та осалювання
За окиснення жирів втрачається природне забарвлення; специфічний смак і запах продукту; з'являється сторонній, іноді неприємний присмак, аромат; втрачається біологічна цінність.
Первинні продукти окислення – пероксиди – органолептично не можна виявити, проте, за їх вмістом можна зробити висновок про глибину псування жиру, придатність його для тривалого зберігання і споживання.
Вторинні продукти окислення погіршують органолептичні показники жиру. Розрізняють два основні види псування жиру – згіркнення і осалювання.
Згіркнення відбувається в результаті накопичення в жирах низькомолекулярних продуктів: альдегідів, кетонів, низькомолекулярних жирних кислот. В цьому випадку жир набуває згірклого смаку і різкого, неприємного запаху. Згіркнення жирів може відбуватися внаслідок хімічних і біохімічних процесів.
В процесі хімічного згіркнення, що відбувається в жирах під дією кисню повітря, накопичуються вільні жирні кислоти, іноді низькомолекулярні, не властиві цьому жиру, збільшується пероксидне число, утворюються леткі карбонільні сполуки (альдегіди і кетони). Саме ці сполуки надають запах згірклості жиру.
В процесі біохімічного згіркнення, що відбувається за участі ферментів плісняви, утворюються кетокислоти і метилалкілкетони в результаті β-окиснення вільних жирних кислот, що утворюються під час гідролізу під впливом ліпаз. В результаті чого з кислот утворюється кетон, що містить на один атом вуглецю менше, ніж в початковій кислоті: з капронової – метилпропілкетон, каприновою – метилгептилкетон, лауриновою – метилнонілкетон і т.д. Кетонне згіркнення іноді називають "духмяним згіркненням" у зв'язку зі своєрідним запахом продуктів окиснювального псування.
Осалювання жирів супроводжується зникненням забарвлення, ущільненням жиру і появою сальної консистенції в результаті окислювальних змін жиру. Під час осалювання утворюється значна кількість оксисполук в результаті розпаду на світлі первинних органічних пероксидів і появи вільних радикалів ![]() ОН і НО
ОН і НО![]() за фотохімічної дії на жир. Радикали, що виникають взаємодіють з молекулами жирних кислот з утворенням оксикислот. Кількість їх визначають за ацетиловим числом, яке зростає зі збільшенням кількості оксигруп.
за фотохімічної дії на жир. Радикали, що виникають взаємодіють з молекулами жирних кислот з утворенням оксикислот. Кількість їх визначають за ацетиловим числом, яке зростає зі збільшенням кількості оксигруп.
Оксикислоти, що утворилися, залучаються до процесу полімеризації, внаслідок чого утворюються високомолекулярні сполуки і жир набуває характерної сальної мазеподібної консистенції. Жир, що засалився, характеризується також специфічним неприємним запахом і смаком.
Зміна забарвлення жирів пов'язана з руйнуванням каротиноїдів, яке настає до початку окиснювальних змін. Жир, що знебарвлюється, інколи набуває зеленуватого забарвлення, змінюється його спектр поглинання. Ці зміни каротиноїдів дозволяють виявити окиснювальні зміни жирів на ранніх стадіях. Відбувається також і розпад токоферолів.
Найбільш інтенсивно окиснювальне псування відбувається за тривалого нагріванні жирів за високих температур 180°С...300°С. Таке нагрівання супроводжується зниженням вмісту ненасичених жирних кислот і накопиченням пероксидів, карбонільних сполук, летких кислот і продуктів сополімеризації.
Термічне розкладання жирів
За температури понад 200°С може статися термічне розкладання жиру з виділенням диму (піроліз). Температура, за якої починається виділення диму, називається температурою (або точкою) димоутворення, або піролізу. На величину цієї температури впливає вид жиру, вміст вільних жирних кислот, матеріал і розмір посуду, наявність металів й інші чинники. Наприклад, збільшення у свинячому жирі вмісту вільних жирних кислот з 0,02 до 0,81% зменшує температуру піролізу з 221 до 150°С. Залізо і мідь каталізують піроліз жиру.
Продукти піролізу погіршують колір жиру під час смаження харчових продуктів. Потемніння жиру відбувається за рахунок забруднення його речовинами пірогенетичного розпаду, дрібних частинок, що утворюються в процесі обвуглювання, реакцій меланоїдиноутворення і карамелізації, а також накопичення темнозабарвлених продуктів окислення самого жиру.
Зміна запаху жиру за тривалого смаження продуктів викликана утворенням акролеїну. Карбонільні сполуки, що утворюються під час смаження, містять 3, 5, 7 атомів вуглецю, погіршують запах і смак жиру, а ті, що містять 4, 6, 10, 12 атомів вуглецю надають жиру приємний запах смаженого.
Зміна біологічної цінності жиру
В результаті окиснення змінюються не лише органолептичні властивості жиру, але і знижується його харчова, у тому числі біологічна цінність. Це пов'язано з окисненням життєво необхідних ненасичених жирних кислот, а також з руйнуванням каротиноїдів, токоферолів, фосфатів і інших біологічно активних речовин. Крім того, первинні продукти окиснення, пероксиди справляють токсичну дію на організм. В той же час пероксиди в процесі різноманітних реакцій утворюють речовини, що містять карбоніли, а також полімерні сполуки, які погіршують засвоюваність жиру, знижуючи його біологічну цінність, а іноді мають канцерогенні властивості. Накопичення таких продуктів специфічного складу і будови відбувається найбільш інтенсивно за тривалого нагрівання жиру за високих температур – вище 180ºС.
Для запобігання окиснювальним процесам в жирах необхідно зменшити або виключити контакт жиру передусім з киснем повітря. Без доступу кисню навіть тривале нагрівання за 180ºС...190ºС не викликає помітних окислювальних змін жиру. Збільшенню контакту з повітрям сприяє нагрівання жиру тонким шаром, смаження продуктів пористої структури, сильне спінювання і перемішування жиру.
Для стабілізації фрітюрних жирів застосовують кремнійорганічні рідини (поліметилсилоксани). Ці сполуки, утворюючи на поверхні жиру тонку плівку і пригнічуючи його спінювання, утруднюють взаємодію жиру з киснем.
Жир доцільно зберігати в герметичній тарі, у вакуумній упаковці або в атмосфері інертного газу за від’ємних температур. У жирах не повинно бути легкоокиснювальних металів (міді, заліза, марганцю), їх солей або органічних похідних сполук свинцю, олова і інших металів. Для уповільнення окислювальних процесів в жирах застосовують антиоксиданти.
Висихання жирів
Рідкі жири, намазані тонким шаром поводяться на повітрі по-різному: одні залишаються без зміни рідкими, інші, окиснюючись, поступово перетворюються на прозору смолоподібну еластичну плівку – ліноксин, нерозчинну в органічних розчинниках. Олії, що не утворюють плівку, називаються невисихаючими. Головною складовою частиною в таких оліях є гліцериди олеїнової кислоти (з одним подвійним зв'язком). Олії, що утворюють щільну плівку, називаються висихаючими. Головною складовою частиною в таких оліях є гліцериди ліноленової кислоти (з трьома подвійними зв'язками). Олії, що утворюють м'які плівки, називаються напіввисихаючими. Головною складовою частиною в таких оліях є гліцериди лінолевої кислоти (з двома подвійними зв'язками). Здатність деяких олій до висихання широко використовується в народному господарстві (лакофарбна промисловість). Для медицини, навпаки, представляють інтерес олії невисихаючі, оскільки вони використовуються для парентерального введення лікарських засобів.
Надійним способом виявлення висихаючості олій є визначення йодного числа, за яким можна легко встановити, до якої групи за ступенем висихаючості відноситься та або інша олія (таблиця 4.3).
Таблиця 4.3 – Значення йодного числа для олій з різною здатністю до висихання
|
Назва кислоти |
Йодне число деяких олій |
|
Невисихаючі олії(тип олеїнової кислоти) |
|
|
Оливкове |
80-85 |
|
Арахісове |
83-105 |
|
Мигдальне |
93-102 |
|
Персикове |
96-103 |
|
Касторове |
81-90 |
|
Напіввисихаючі олії(тип лінолевої кислоти) |
|
|
Гірчичне |
93-107 |
|
Кунжутне |
103-112 |
|
Бавовняне |
100-120 |
|
Соняшникове |
119-144 |
|
Кукурудзяне |
111-131 |
|
Висихаючі олії(тип ліноленової кислоти) |
|
|
Макове |
131-143 |
|
Конопляне |
140-175 |
|
Льняне |
169-192 |
Олеїнова кислота має здатність під впливом азотистої кислоти переходити у свої стереоізомер – елаїдинову кислоту, яка за кімнатної температури має тверду консистенцію. Цю реакцією, відомою під назвою елаїдинова проба, широко використовують для визначення типу олії: якщо проба позитивна, то досліджувана олія є невисихаючою (містить тригліцериди олеїнової кислоти).