1.2 Теоретичні відомості
Вода є важливою складовою харчових продуктів. Вона міститься в рослинних і тваринних продуктах як клітинний і позаклітинний компонент, як диспергувальне середовище і розчинник, що зумовлює консистенцію і структуру харчових продуктів, впливає на їх зовнішній вигляд, смак та стійкість продуктів в процесі зберігання. Кількість вологи в продукті визначає його енергетичну цінність, оскільки чим більше в ньому міститься води, тим менше корисних сухих речовин (білків, жирів, вуглеводів та ін.) в одиниці маси. З вмістом води тісно пов’язана стійкість продукту під час зберігання та його транспортабельність, а також придатність до подальшої переробки, так як надлишок вологи сприяє перебігу ферментативних і хімічних реакцій, активізує діяльність мікроорганізмів, в тому числі таких, які призводять до псування продукту, зокрема його пліснявіння. В зв’язку з цим вміст вологи в продукті визначає умови та строки його зберігання.
ПОКАЗНИКИ ВМІСТУ ВОДИ В ХАРЧОВИХ ПРОДУКТАХ
Вміст вологи у матеріалі характеризується показником масової частки вологи W – це виражене у відсотках відношення різниці мас зразка продукту до і після висушування до маси зразка до висушування
![]() , (1.1)
, (1.1)
де m1 – маса наважки до висушування, г; m2 – маса наважки після висушування, г.
Масова частка вологи в харчових продуктах змінюється в широких межах, %:
|
м'ясо................... |
65…75% |
молоко...................... |
87…88% |
|
часник................. |
65% |
огірки....................... |
90% |
|
хліб....................... |
35…50% |
мед........................... |
20% |
|
фрукти, овочі..... |
65…95% |
маргарин.................. |
16…17% |
|
борошно............. |
12…15% |
кава у зернах............. |
5% |
|
сухе молоко......... |
4% |
цукор-пісок............... |
0,14…0,15% |
|
пиво, соки............ |
87…90% |
олія........................... |
0,1% |
|
сир твердий........ |
37% |
вершкове масло........ |
16…20% |
|
сир м’який.......... |
65…80% |
|
|
Вміст вологи у готових виробах впливає на вихід продукції. Зі збільшенням кількості вологи вихід виробів зростає. Особливо цей фактор необхідно враховувати на хлібопекарських підприємствах, тому що збільшення масової частки вологи борошна на 1 % знижує вихід хліба на 1,5…2 %, а підвищення вологості м’якушки хліба на 1 % призводить до підвищення його виходу на 2…3 %.
Враховуючи важливість цього показника, відповідні стандарти (ДСТУ) та технічні умови (ТУ) встановлюють норми вмісту вологи, а також методи її визначення, що робить обов’язковим знаходження цього показника під час контролю якості сировини та готових виробів.
СТАН ВОДИ В ХАРЧОВИХ ПРОДУКТАХ
Загальна вологість продукту вказує на кількість вологи в ньому, але не характеризує її причетність до хімічних, біохімічних і мікробіологічних змін в продукті. У забезпеченні його стійкості під час зберігання важливу роль відіграє співвідношення вільної і зв'язаної вологи.
Зв'язана волога – це асоційована вода, міцно зв'язана з різними компонентами – білками, ліпідами і вуглеводами за рахунок хімічних і фізичних зв'язків. Така вода існує поблизу розчиненої речовини й інших неводних компонентів, має зменшену молекулярну рухливість та інші властивості, що відрізняються від усієї маси води в тій же системі, і не замерзає за температури -40ºС.
Вільна волога – це волога, яка не зв'язана полімером і доступна для перебігу біохімічних, хімічних і мікробіологічних реакцій.
Наприклад, за вологості зерна 15...20% зв'язана вода складає 10...15%. За більшої вологості з'являється вільна волога, що сприяє посиленню біохімічних процесів (наприклад, проростанню зерна).
Плоди і овочі мають вологість 75...95%. В основному, це вільна вода, проте приблизно 5% вологи утримується клітинними колоїдами в міцно зв'язаному стані. Тому овочі і плоди легко висушити до 10...12%, але висушування до нижчої вологості вимагає застосування спеціальних методів.
Більша частина води в продукті може бути перетворена на лід за температури -5°С, а вся – за температури -50ºС і нижче. Проте певна частка міцно зв'язаної вологи не замерзає навіть за температури -60ºС.
Зрозуміло, що на видалення вільної і зв’язаної вологи затрати енергії будуть різні.
Вільна вода слабко зв'язана з сухими речовинами, легко видаляється з продукту під час висушування (t ~ 100º С), віджимання, пресування, замерзає за 0ºС. Різновидом вільної води є гігроскопічна, поглинена продуктами з повітря. Продукти, що мають здатність поглинати або віддавати вологу, називаються гігроскопічними (цукор, цукристі кондитерські вироби, крупа, борошно, крохмаль, сушені плоди й овочі).
Зв'язана вода міцно утримується сухими речовинами і погано видаляється навіть випаровуванням (t > 300ºС). Зв'язана вода знаходиться в мікрокапілярах, адсорбується внутрішньоклітинними системами і утримується колоїдами білків і вуглеводів. До зв'язаної води відноситься також кристалізаційна вода. Наприклад, вода, що входить до складу кристалів лимонної кислоти і глюкози (С6Н12О6 ·Н2О). Таку воду можна видалити з продукту в результаті термічного розкладання деяких речовин за підвищених температур. Зв'язана вода має інший показник заломлення, має нижчу температуру замерзання, густину, не засвоюється мікроорганізмами і позитивно впливає на збереження продукту.
Вода зв'язана може переходити у воду вільну і навпаки. Наприклад, під час розмерзання м'яса, риби, свіжих плодів і овочів частина зв'язаної води переходить у вільну, що призводить до псування продуктів під дією мікроорганізмів. Під час замішування тіста, варіння макаронних виробів вільна вода поглинається білками і перетворюється на зв'язану колоїдними системами воду.
Поділ на зв’язану і незв’язану воду є умовним, так як майже вся вода, що міститься в харчовому продукті знаходиться у зв’язаній формі, але утримується тканинами з різною силою. Так, за класифікацією П.А. Ребіндера (для колоїдних капілярно-пористих тіл), в основу якої покладена природа та енергія хімічного зв’язку форми зв’язку вологи з сухими речовинами поділяються на три групи: хімічна, фізико-хімічна і фізико-механічна.
1. Хімічна форма зв'язку – молекули води входять до складу речовин в точному кількісному співвідношенні. Для видалення її потрібно інтенсивну обробку теплом, що призводить до руйнування структури матеріалу(зв'язана вода).
2. Фізико-хімічна форма зв'язку – адсорбційна й осмотична. Адсорбційно-зв'язана вода утримується силами Ван-дер-Ваальса поверхневих молекул колоїдних речовин (білків і вуглеводів) на межі поділу тверде тіло-вода. Наприклад, в зернових культурах за їх вологості менше 14% вода знаходиться в зв'язаному стані. З підвищенням вологості 14,5-15,5% з'являється вільна вода. Подальше поглинання води зумовлюється силами осмосу і дифузії. Така вода називається осмотично поглиненою або структурною. Вона не так міцно зв'язана, характеризує стадію набрякання (вільна вода).
3. Фізико-механічна форма зв'язку характерна для води, що заповнює капіляри, великі пори і порожнини в тілах. Капілярами вода утримується з більшою силою (зв'язана вода). Волога, що утримується силами зчеплення, зв'язана з матеріалом найслабкіше і може бути видалена механічним шляхом (вільна вода).
Стан води в харчових продуктах, її причетність до хімічних та біологічних змін характеризується таким показником як активність води.
Активність води aw – це відношення тиску пари води над продуктом (Pw) до тиску пари води над чистою водою (Р0) за тієї ж температури:
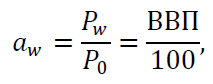 (1.2)
(1.2)
де – ВВП відносна вологість продукту в стані рівноваги, коли продукт не сприймає вологу і не віддає її в атмосферу.
Показник активності води (таблиця 1.1) краще характеризує вплив вологи на псування продукту ніж просто значення вмісту вологи. За величиною aw розрізняють:
– продукти з високою вологістю aw = 1,0...0,9;
– продукти з проміжною активністю aw = 0,9...0,6;
– продукти з низькою активністю aw = 0,6...0,0.
Таблиця 1.1 – Активність води (аw) в харчових продуктах
|
Продукт |
Вологість, % |
aw |
Продукт |
Вологість, % |
aw |
|
Фрукти |
90-95 |
0,97 |
Борошно |
16-19 |
0,80 |
|
Яйця |
70-80 |
0,97 |
Мед |
10-15 |
0,75 |
|
М'ясо |
60-70 |
0,97 |
Карамель |
7-8 |
0,65 |
|
Сир |
40 |
0,92-0,96 |
Печиво |
6-9 |
0,60 |
|
Джем |
30-35 |
0,82-0,94 |
Шоколад |
5-7 |
0,40 |
|
Хліб |
40-50 |
0,95 |
Цукор |
0-0,15 |
0,10 |
|
Кекс |
20-28 |
0,83 |
|
|
|
Вода в продуктах харчування її вміст та активність є найважливішими чинниками, що впливають на стійкість продуктів під час зберігання. Так, в продуктах з низькою вологістю можуть відбуватися процеси окиснення жирів, неферментативне потемніння, втрата водорозчинних речовин, ферментативне псування; в продуктах з проміжною вологістю – ті ж процеси, а також процеси за участі мікроорганізмів; в продуктах з високою вологістю – вирішальна роль належить процесам за участі мікроорганізмів.
Більшість бактерій розмножується за aw = 0,85...0,95; плісняв – за aw = 0,6...0,8; дріжджів – aw = 0,8...0,9.
Активність води має велике значення і для текстури продуктів. Наприклад, в сухих продуктах (сухе молоко, крекери і т.п.) максимальне значення aw повинно бути 0,35...0,5. Для продуктів з м’якою текстурою, що не повинні хрумтіти значення aw мають бути більшими.
В країнах Євросоюзу показник активності води є обов’язковим під час проведення експертизи цілого ряду харчових продуктів.
МЕТОДИ ВИЗНАЧЕННЯ МАСОВОЇ ЧАСТКИ ВОЛОГИ В ХАРЧОВИХ ПРОДУКТАХ
Методи визначення вологи поділяються на дві групи: прямі і непрямі (рисунок 1.1). Прямі методи засновані на розділенні матеріалу на суху речовину і воду, використовуючи тепло, безводні розчинники і хімічні реактиви. Непрямі методи ґрунтуються на вимірюванні зміни фізичних величин і властивостей, функціонально пов'язаних з вологістю матеріалів.
До прямих методів відноситься: відгонка – дистиляція води з наважки із застосуванням органічних рідин, що мають високі температури кипіння з наступним визначенням об’єму перегнаної води; хімічні – взаємодія води з яким-небудь реагентом; теплофізичні – засновані на випаровуванні води з наважки аналізованого матеріалу. Прямі методи громіздкі, складні, потребують великих затрат часу та праці, непридатні для оперативного контролю.
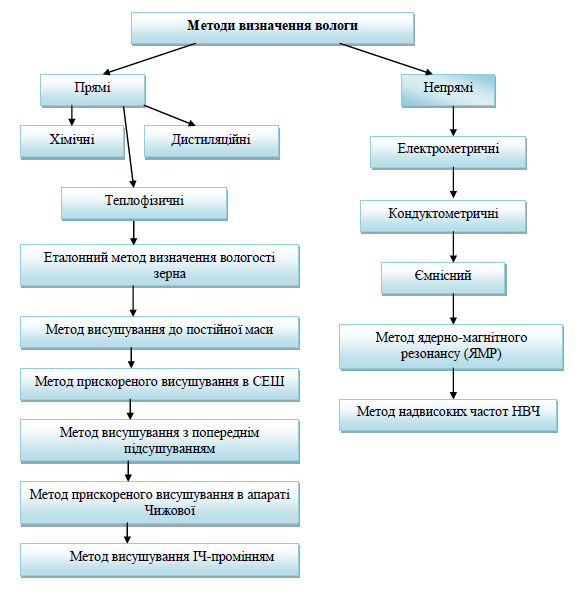
Рисунок 1.1 – Методи визначення масової частки вологи в харчових продуктах
Дистиляційні методи засновані на відгоні гігроскопічної води з узятої наважки продукту і визначенні її кількості. Воду з аналізованого зразка відганяють разом із органічним розчинником, що не змішується з водою і не реагує хімічно з досліджуваною речовиною. Найчастіше використовують бензин, з якого відігнані легкі фракції, що киплять до 95ºС. Рідше застосовують бензол (Ткип = 80,2ºС), толуол(Ткип = 110,8ºС), ксилол (Ткип = 138ºС) та ін.
Наважку заливають в колбі органічною рідиною. Під час змішуванні води з вказаними органічними речовинами виходять азеотропні суміші. Температура кипіння суміші є нижчою за температуру кипіння компонентів: води (Ткип = 100º С) з толуолом – +88ºC, води з ксилолом – +92ºС. Відгін води закінчується за 10...20 хвилин. Відігнану воду з частиною органічного розчинника збирають в приймальній посудині для розділення рідин, що не змішуються і визначають кількість відігнаної води. Перевага методу – знижується можливість розкладання органічних речовин, і органічна рідина оберігає висушений матеріал від окислення. Метод застосовують для визначення вологи в прянощах і приправах.
Дистиляційні методи поділяються на дві групи: прямого визначення і відкритої дистиляції.
За методом прямого визначення суміш пари води і рідини, що не змішуються з нею, конденсують, дистилят збирають в градуювальний приймач, де проходить розшарування його на 2 шари, і за межею розділу двох рідин визначають об'єм води, відігнаний з узятого матеріалу наважки. Вимоги до органічної речовини: не змішується з водою і хімічно інертна по відношенню до речовин, що входять до складу аналізованої речовини. Температура кипіння органічної рідини має бути більше температури кипіння води.
За методом відкритої дистиляції А.Г. Кульмана вологість матеріалу визначають за спадом маси після нагрівання аналізованого матеріалу в середовищі висококиплячих речовин, маса яких за нагрівання не змінюється. Використовуються рослинні і вазелінові олії, парафін. Метод заснований на нагріванні наважки досліджуваного продукту зі зневодненою рослинною олією за температури 160...170°С впродовж декількох хвилин. Втрата маси, що відбувається при цьому, приймається за вологість.
Визначення ведеться таким чином: в металевий тигель, абсолютно чистий і сухий, вносять 20...22 см3 рослинної олії (чи бавовняного, парафіну, сало-масла), вкладають в тигель термометр-паличку і зважують на технохімічних вагах з точністю до 0,01 г (тара). Після цього в тигель вносять 5 г досліджуваної речовини, заздалегідь підготовленої для аналізу і знову зважують. За різницею між першим і другим зважуваннями знаходять точну величину узятої наважки.
Перемішують вміст тигля термометром, поміщають тигель на розігріту піщану баню і нагрівають з таким розрахунком, щоб вміст тигля нагрівся до 165° впродовж 4...5 хвилин, після чого за цієї температури витримують тигель впродовж 3...5 хв., в залежності від досліджуваного об'єкта. Під час нагрівання коливання температури вмісту тигля допускається в межах ± 5°С.
Потім знімають тигель з вогню, дають йому трохи охолонути, після чого дно тигля занурюють у холодну воду і охолоджують до кімнатної температури (18-20°). Обтерши до суху тигель, його зважують.
Кількість вологи в досліджуваній речовині знаходять за формулою:
![]() , (1.3)
, (1.3)
де – а – маса тигля з олією, термометром і наважкою до нагрівання, г; b – маса тигля з олією, термометром і наважкою після нагрівання, г; g – маса наважки, г.
Після кожного визначення вміст тигля зливають в суху склянку з притертою пробкою; коли залишків збереться достатня кількість, вміст склянки підігрівають до 80-100° З(на водяній бані) і фільтрують олію. Цю зневоднену олію можна використати для подальших визначень.
Ці методи доцільно використовувати для визначення масової частки вологи в харчових продуктах, які містять багато жиру, летких речовин, вуглеводів, здатних до карамелізації (наприклад, прянощі, риба копчена і солона, морські водорості, сухофрукти та ін.).
Хімічні методи засновані на здатності деяких реагентів (лужних металів, карбіду кальцію та ін.) вступати в хімічну взаємодію з водою. Кількість води знаходять за еквівалентним обсягом газу (водню, ацетилену), що виділився під час реакції. Проте через трудомісткість й інші причин ці методи не отримали застосування.
Використовується титриметричний метод К. Фішера, в основу якого покладена відкрита Бунзеном реакція йоду з водою у присутності діоксиду сірки.
Титрування за модифікованим методом Карла Фішера. Окисно-відновна реакція йоду і діоксиду сірки перебігає у присутності води:
J2+SO2+2H2O→2HJ+H2SO4.
Кислотні продукти, що накопичуються в середовищі, перетворюють цю реакцію на оборотну:
2HJ+H2SO4 →J2+H2SO3+H2O,
що утруднює визначення кінця реакції. Для зв'язування кислотних продуктів і усунення оборотності реакції готують розчини йоду і діоксиду сірки в органічній основі.
Використання спеціально підібраних органічних реагентів дозволяє досягти повного витягання води з харчового продукту. Вміст вологи в продукті розраховується за кількістю йоду, витраченій на титрування. Метод відрізняється високою точністю і стабільністю результатів (у тому числі за дуже низького вмісту вологи) і швидкістю проведення аналізу.
Реактив Фішера є розчином I2 і SO2 в піридині і метанолі. Отримують його розчиненням сублімованого йоду в суміші безводного піридину і абсолютного метанолу. Розчин охолоджують льодом і додають рідкий або газоподібний діоксид сірки (співвідношення SO2 : I2 = 1:1.3). Реактив взаємодіє з водою за схемою:
PySO2 + CH3OH ↔ PyH+–CH3SO3–
PyH+–CH3SO3– + PyI2 + H2O + Py → 2(PyH+I–) + PyH+CH3SO4–
Піридин необхідний для зв'язування кислих продуктів реакції і створення оптимального рН в інтервалі 5...8. Реактив Фішера застосовують для прямого і зворотного титриметричного визначення води. Точку еквівалентності встановлюють за появою або зникненням забарвлення йоду методом амперометрії або потенціометрії. У поширеному кулонометричному варіанті титрування здійснюють йодом, що електрогенерується, в розчині, що містить, I, SO2, піридин і метанол.
Використовують різні модифікації реактиву. Так, замість піридину застосовують діетаноламін або імідазол, замість йоду і піридину – суміш ацетату натрію з йодидом калію або натрію (так званий ацетатний реактив Фішера), замість метанолу – метил або етилцелюлоза.
За допомогою реактиву Фішера визначають вміст води (не менше 5(10-6%) не лише в продуктах харчування, але і в нафті, лаках, фарбах, лікарських засобах та ін. Реактив непридатний для визначення вологості окисників і відновників, що реагують з його компонентами з поглинанням або виділенням води або йоду.
Найпоширенішим серед прямих методів є метод визначення масової частки вологи за сухим залишком, тобто коли кількість вологи встановлюють за різницею у масі наважки до та після сушіння. Існує багато модифікацій цього методу (рисунок 1.1), які відрізняються тривалістю та температурою нагрівання наважки цілого чи подрібненого зразку, а також ступенем його подрібнення. Можливі випадки, коли продукт із надмірним вмістом вологи перед висушуванням піддають попередньому підсушуванню. Для прискорення висушування, а також для висушування речовин, що легко розкладаються за температури вище 100ºС, процес проводять за пониженого тиску, що дає можливість знизити температуру. Для в’язких продуктів (меляса, цукровий сироп та ін.) висушування утруднюється за рахунок утворення на його поверхні твердої скоринки. Для полегшення і прискорення процесу висушування в використовують наповнювачі (на 1 г в’язкого продукту беруть 25 г наповнювача), в результаті змішування з якими в’язкі продукти стають пухкими. В якості наповнювачів використовують прожарений кварцовий або звичайний річковий пісок. Інколи для висушування в’язких рідин використовують ролики із фільтрувального паперу. Однак ці методи мають недоліки, так як у випадку їх використання визначається не справжня масова частка вологи, а її умовна величина, що залежить від прийнятого методу визначення.
Явища, що відбуваються в об’єкті під час висушування, особливо в харчових продуктах, є дуже складними. Під дією теплоти видаляється волога та одночасно деяка кількість сухих речовин внаслідок розкладання органічних речовин під дією високої температури. Поряд з цим в об’єкті, що висушується можуть відбуватися окиснювальні і гідролітичні процеси, внаслідок чого збільшується його маса.
Процес висушування залежить від стану вологи в дослідному матеріалі, яка може бути вільною або зв’язаною з матеріалом різними видами зв’язків:
– хімічним – видалити таку вологу можна лише руйнуванням продукту шляхом прожарювання або хімічної дії;
– фізико-хімічним (адсорбційним, осмотичним, структурним) – видалити вологу можна висушуванням об’єкта, причому легше видаляється осмотична волога (волога набухання), ніж адсорбційна (утримується силовим полем молекул);
– механічним (волога макро-, мікрокапілярів, а також волога на поверхні) – видаляється найлегше під час висушування.
Методи визначення масової частки вологи висушуванням є найбільш поширеними та універсальними. Їх недоліком є те, що дуже важко видалити всю воду з харчового продукту, особливо колоїдно-зв’язану.
Серед цих методів слід виділити наступні два методи: висушування до постійної маси за температури 100…105 °С та прискорене висушування за підвищених температур (130…160 °С). Перший метод дає найбільш точні результати, оскільки висушування відбувається необмежений час, на відміну від прискореного способу, а до повного видалення вологи. Однак він досить тривалий та трудомісткий, тому під час контролю виробництва використовують ряд прискорених методів.
Прискореними методами визначають масову частку вологи в зерні (ДСТУ 13586.5-93), крохмалі (ГОСТ 7699-78 та ГОСТ 7697-82), макаронних виробах (ГОСТ 14849-69) і т.д. Для кожного продукту в залежності від фізико-хімічних властивостей підібрані своя температура висушування та тривалість процесу. Найчастіше тривалість висушування складає 50 хв. Прискорення висушування робить ці методи більш умовними, так як розкладання речовин за високої температури протікає більш енергійно. Крім цього, застосування прискореного методу висушування до об’єктів з підвищеною вологістю, наприклад до хліба, дає явно занижені результати через недосушування продукту. На результати аналізу впливають також коливання температури, тривалість висушування, конструктивні особливості сушильної шафи, розміри та форма бюкси.
Метод висушування до постійної маси (у сушильній шафі СЕШ за t=105ºС). Наважку об'єкту дослідження масою 3...10 г зважують на аналітичних вагах з точністю до 0,001 г, в заздалегідь висушені, охолоджені в ексикаторі і зважені бюкси, заввишки не більше 30 мм, діаметром 45 мм. Об'єкт зважують в закритих бюксах. Бюкси відкривають і поміщають в сушильну шафу або вакуум-сушильну шафу за можливості ближче до термометра. У сушильній шафі наважку висушують за температури 100...105°С, а у вакуум-сушильній – за температури 100°С (тиск підтримують ≈ 700 мм рт.ст.). Висушування в обох випадках починають за температури 50°С і, поступово підвищуючи температуру, досягають 100...105°С приблизно через 30 хв. Через 1,5-3 год бюксу зважують перший раз. Заздалегідь її охолоджують в ексикаторі над концентрованою сірчаною кислотою або прожареним хлористим кальцієм. Потім відкривають бюкси і знову поміщають їх в сушильну шафу. Подальші зважування роблять через 1 год. Висушування і зважування повторюють до тих пір, поки різниця в масі не досягне 0,001 г. Зазвичай тривалість висушування складає 3...5 год вміст вологи обчислюють за формулою:
![]() (1.4)
(1.4)
де - W – вміст вологи в об'єкті %; m – маса бюкса, г; m1 – маса бюкса з наважкою до висушування, г; m2 – маса бюкса з наважкою після висушування, г.
Метод прискореного висушування в СЕШ (температура підвищується до 130ºС, менш тривалий спосіб).
Двохетапне висушування. Оскільки харчові продукти представляють, у більшості випадків, біоколоїди і погано піддаються висушуванню, то для тих з продуктів, які особливо багаті вологою (фрукти, овочі, хліб, м'ясо та ін.), рекомендується вести висушування в два етапи: спочатку взяту наважку (10...20 г) розрізають на тонкі шматки і висушують за кімнатної температури (інколи в сушильній шафі) до повітряно-сухого стану, оберігаючи наважку від можливих забруднень. Пробу потім зважують, після чого невелику наважку (3...5 г) подрібнюють і досушують в шафі до постійної ваги за температури 105ºС.
Метод висушування в приладі К.Н. Чижової (висушування матеріалу здійснюється шляхом передачі тепла від щільно прилеглих до нього плит, що нагріваються електрикою, зазвичай за температури ~ 160ºС протягом ~ 3 хв.).
Метод висушування ІЧ-променями. ІЧ-промені – електромагнітне випромінювання, що випромінюється нагрітими тілами, тому ІЧ-промені називаються тепловими променями. Вода здатна майже повністю поглинати усі теплові промені (95-96%), що падають на неї, швидко нагріваючись і випаровуючись. Метод заснований на високій здатності вологих матеріалів поглинати потужний тепловий потік ІЧ-випромінювання, час висушування значно скорочується (25 хв.). Метод використовується в приладах-вологомірах – сушильна камера , яка з’єднана з вагами. Шкала ваг градуйована так, що показує пониження маси наважки за рахунок випареної води.
Ліофільне висушування. В основу методу покладене випаровування (сублімація) льоду без проміжного утворення води. Метод застосовують для продуктів, що міцно утримують воду (речовини, багаті білками, полісахаридами та ін.) Висушування ведеться у вакуумі, але за умови попереднього заморожування узятої для аналізу проби. Досліджуваний продукт шаром завтовшки не більше 10 мм піддається заморожуванню в посудині за допомогою вугільного ангідриду. Потім посудину швидко переносять в ексикатор, помістивши посудину на пробку для зменшення теплопровідності. За допомогою насосу створюють в ексикаторі вакуум. Випаровування води можна прискорити, якщо заморожений матеріал опромінювати сильним світлом. Висушування закінчується приблизно за 4 години, якщо заморожений шар має товщину 1...2 мм; шар завтовшки 10 мм слід висушувати впродовж 24 годин. Іноді для видалення залишкової вологи зразок висушують у вакуум-ексикаторі над Р2О5. Вміст вологи обчислюється за зміною маси.
На відміну від прямих, непрямі методи дозволяють швидко отримувати інформацію про масову частку вологи у матеріалі та автоматизувати процес вимірювання масової частки вологи. В непрямих методах визначається не сама волога в дослідному об’єкті, а показник, функціонально пов’язаний з масовою часткою вологи матеріалу.
До непрямих методів відносяться:
– фізичні – визначення масової частки сухих речовин за величиною відносної густини чи рефрактометрично;
– електричні – визначення масової частки вологи за електропровідністю або електричною проникність
Серед непрямих методів практичне застосування в харчовій промисловості отримали електрохімічні методи, в яких вимірюють електропровідність і діелектричну проникність.
Кондуктометричний метод заснований на залежності електричного опору матеріалу від ступеня його вологості: чим більше вологості, тим менше питомий опір матеріалу і тим більше його електропровідність. Ступінь дисоціації молекул органічних речовин дуже низький, тому в сухому стані вони є діелектриками, що погано проводять електричний струм. У випадку зволоження матеріалу його електропровідність збільшується (рисунок 1.2) за рахунок розчинення у воді мінеральних солей, що містяться в матеріалі, здатних майже повністю дисоціювати на іони, які є гарними провідниками електричного струму.
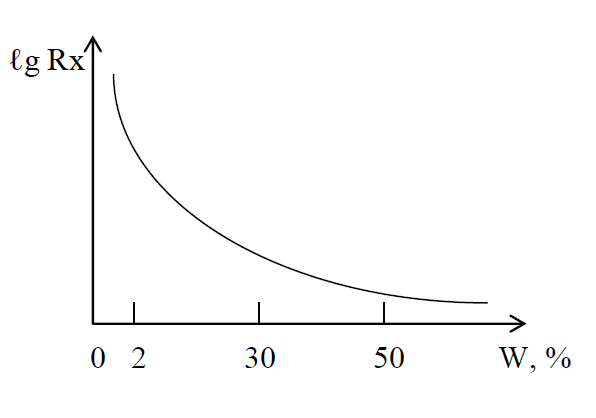
Рисунок 1.2 – Залежність електропровідності матеріалу (Rx) від масової частки вологи (W)
В результаті цього питомий опір матеріалу зменшується на 12...18 порядків. Метод застосовується за низької та середньої вологості матеріалу(~ до 18...20%). Незначне збільшення вологості призводить до значного зменшення опору(крива круто падає).
У лабораторному контролі використовують вологоміри, що працюють за принципом вимірювання електропровідності.
Ємнісний метод заснований на залежності величини діелектричної проникності (ДП; ε) матеріалу від вмісту в ньому води. ε=81, ДП сухої речовини ~ 3...5, отже підвищення вологості призводить до збільшення ДП.
Метод надвисоких частот(НВЧ) заснований на поглинанні водою енергії, що збуджується генератором НВЧ-випромінювання.
Рефрактометричний метод. Принцип методу заснований на зміні показника заломлення розчинів в залежності від кількості розчинених в них сухих речовин. Цим методом визначають кількість води в сиропах, соках, настоях та ін.).
ВИЗНАЧЕННЯ СПІВВІДНОШЕННЯ ВІЛЬНОЇ І ЗВ'ЯЗАНОЇ ВОЛОГИ
Диференціальна скануюча калориметрія. Якщо зразок охолодити до температури менше 0ºС, то вільна волога замерзне, зв'язана – ні. За нагрівання замороженого зразка в калориметрі можна виміряти тепло, що поглинулось під час танення льоду. Незамерзаюча вода визначається як різниця між загальною і замерзаючою водою.
Термогравіметричний метод. Метод заснований на визначенні швидкості висушування. У контрольованих умовах межа між ділянкою постійної швидкості висушування і ділянкою, де ця швидкість знижується, характеризує зв'язану вологу.
Діелектричні вимірювання. Метод заснований на тому, що за 0ºС значення діелектричної проникності води і льоду є приблизно однаковими. Але якщо частина вологи зв'язана, то її діелектричні властивості повинні сильно відрізнятися від діелектричних властивостей об'ємної води і льоду.
Вимірювання теплоємності. Теплоємність води більша, ніж теплоємність льоду, оскільки з підвищенням температури у воді відбувається розрив водневих зв'язків. Цю властивість використовують для вивчення рухливості молекул води. Значення теплоємності води залежно від її вмісту в полімерах дає відомості про кількість зв'язаної води. Якщо за низьких концентрацій вода специфічно зв'язана, то її внесок в теплоємність є незначним. У ділянці високих значень вологості теплоємність в основному визначає вільна волога, внесок якої в теплоємність приблизно в 2 рази більше, ніж льоду.
ЯМР. Метод полягає у вивченні рухливості води в нерухомій матриці. За наявності вільної і зв'язаної вологи отримують дві лінії в спектрі ЯМР замість однієї для об'ємної води.
На рисунку 1.3 показані прилади для визначення зв’язаної води в харчових продуктах за допомогою описаних вище методів.
|
|
|
|
а |
б |
|
|
|
|
в |
|
|
|
|
|
г |
д |
|
а – диференціальний скануючий калориметр DSK; б – термографічний аналізатор; в – прилад для діелектричних вимірювань; г – калориметр; д – прилад для ЯМР-спектроскопії |
|
|
Рисунок 1.3 – Лабораторне обладнання для визначення зв’язаної води у харчових продуктах |
|




